1ro.-¿Que son los compuestos químicos?
los compuestos químicos son la unión de elementos que los podemos ubicar en la tabla periódica de lo elementos químicos un ejemplo claro seria el agua que es la unión de dos elementos que son dos átomos de hidrógeno y uno de oxigeno.
Se los puede describir o mostrar la formula solo con los signos de los elementos de los átomos enlazados según el orden que tienen.
¿cuantos y cuales son los compuestos que conocemos por ahora?
son ocho estos son:
Los principales compuestos químicos que existen en la actualidad son:
- Óxidos básicos
- Óxidos ácidos
- Hidruros:
Son hidruros no metálicos que, cuando se disuelven en agua, adquieren carácter ácido.
- Hidróxidos
- Oxoácidos
- Sales alogenas o neutras. compuestos formados por un hidrácido más un hidróxido.
- Oxisales
Óxidos básicos:
Como ya vimos se obtienen de la union ionica de dos atomos.
metal + oxigeno = óxido básico
- Tradicional: óxido plumboso (cuando el número de oxidación utilizado es el menor), u óxido plúmbico (cuando el número es el mayor).
- Ejemplos:
- óxido cuproso = Cu2 O
- nomenclatura sistemática: necesita de los siguientes vocablos (que irán antes de los nombres de los elementos de la fórmula).Ejemplo:
- mono (1) - hexa (6)
- Numeral de Stock: Exactamente igual que en los casos anteriores, se escribe el óxido normalmente y se le agrega el número de oxidación entre paréntesis.Ejemplo:
- Ni2O3 óxido de Níquel(III)

- Óxidos ácidos:
es un compuesto químico binario que resulta de la combinación de un elemento no metal con el oxígeno.
no metal +oxigeno=oxido ácido
Su nomenclatura solo cambia en la nomenclatura tradicional las demás son iguales.
- Nomenclatura tradicional: Primero se escribe el nombre genérico que en este caso es "anhídrido". El resto del nombre dependerá de la cantidad de estados de oxidación que presente dicho elemento.
- Si presenta un estado de oxidación, continúa el nombre del no metal. Ej: B2O3 = Anhídrido de Boro.
- Si presenta dos estados de oxidación, el nombre del no metal puede terminar en «oso» (si es el menor) o en «ico» (si es el mayor). Ej:el carbono presenta dos estados de oxidación, +2 y +4, en el primer caso: CO = Anhídrido Carbonoso;y en el segundo CO2 = Anhídrido Carbónico.
- Si presenta tres estados de oxidación, el nombre del no metal puede verse modificado de la siguiente manera: ...oso para el menor; ...ico y per...ico para el mayor.
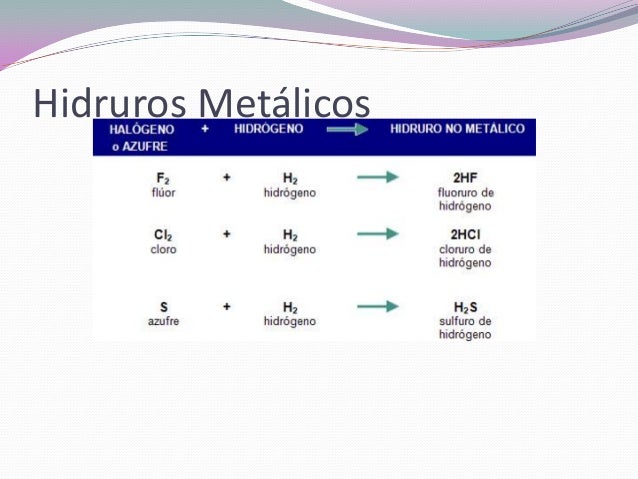
- Hidruros:
Un hidruro es un compuesto químico formado por un cualquier elemento y un hidrógeno. Se dividen en hidruros metálicos, los cuales se forman con un metal + un hidrógeno. Y los hidruros no metálicos los cuales se forman por un no metal + un hidrógeno.
Al igual que los óxidos ácidos solo cambia la nomenclatura tradicional:
- Se formulan escribiendo primero el símbolo del hidrógeno y después el del elemento.Se intercambian las valencias. El hidrógeno actúa con su valencia positiva (+1) y se combina con los elementos .
- Se nombran añadiendo la terminación -uro en la raíz del nombre del no metal y especificando, a continuación, de hidrógeno.
- Es igual tanto en los metales como en los no metales.
- Hidróxidos
Los hidróxidos resultan de la combinación de un óxido básico con el agua.
se clasifican en: básicos, anfóteros y ácidos.
nomenclatura:
Los hidróxidos se formulan escribiendo el metal seguido del grupo dependiente con la base de un ion de radical adecuado con hidroxilo; éste va entre paréntesis si el subíndice es mayor de uno. Se nombran utilizando la palabra hidróxido seguida del nombre del metal, con indicación de su valencia, si tuviera más de una. Por ejemplo, el Ni(OH)2 es el Hidróxido de níquel (II) y el Ca(OH)2 es el hidróxido de calcio (véase Nomenclatura Química).


- Oxoácidos
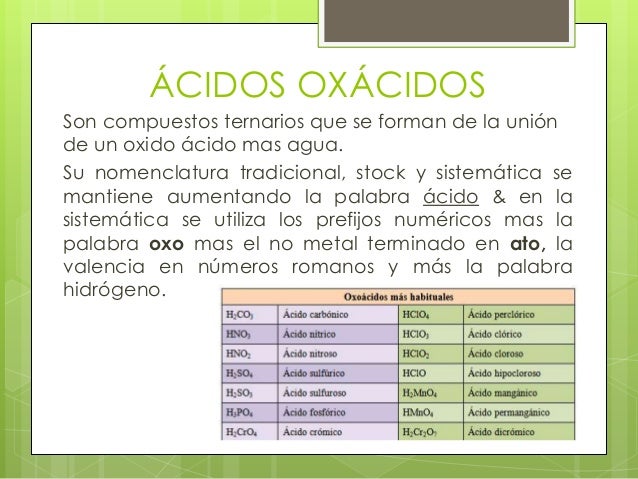

Nomenclatura de los oxoácidos
Para la nomenclatura de los oxoácidos puede utilizarse la nomenclatura tradicional, nomenclatura de stock así como la nomenclatura sistemática.
Nomenclatura tradicional: la nomenclatura tradicional de los oxoácidos se nombra con la palabra ácido seguido de la raiz del elemento no metálico e indicando la valencia con la que actúa según el siguiente criterio.
- Una valencia: Ácido ...ico
- Dos valencias:
- Menor valencia: Ácido ...oso
- Mayor valencia: Ácido ...ico
- Tres valencias:
- Menor valencia: Ácido hipo...oso
- Valencia intermedia: Ácido ...oso
- Mayor valencia: Ácido ...ico
- Cuatro valencias:
- Primera valencia (baja): Ácido hipo...oso
- Segunda valencia: Ácido ...oso
- Tercera valencia: Ácido ...ico
- Cuarta valencia (alta): Ácido per...ico
Ejemplos:
HBrO: ácido hipobromoso
Nomenclatura de stock: la nomenclatura de stock
ácido + perfijo oxígenos + oxo + prefijo X + raíz X + ico + (valecia X)
ácido + perfijo oxígenos + oxo + prefijo X + raíz X + ico + (valecia X)
Ejemplos:
HClO2: ácido dioxoclórico (III)
Nomenclatura sistemática: la nomenclatura sistemática comienza con el prefijo que indica el número de oxígenos seguido de la palabra oxo seguido del prefijo que indica el número de átomos del elemento no metálico (normalmente no se pone porque es 1 átomo) seguido de la raíz del elemento no metálico acabado en ato y en números romanos indicamos la valencia del elemento no metálico seguido de la palabras "de hidrógeno", es decir:
prefijo oxígenos + oxo + prefijo X + raíz X + ato + (valencia X) + de hidrógeno
prefijo oxígenos + oxo + prefijo X + raíz X + ato + (valencia X) + de hidrógeno
Ejemplos:
H2SO2: dioxosulfato de hidrógeno.
- Sales alogenas o neutras.
nomenclatura tradicional:
- indica la valencia del elemento de nombre especifico con prefijos y sufijos
nomenclatura sistematica:
- nombre sustancias usando prefijos que indican la atomicidad de cada uno.Ejemplo:
nomenclatura de stock:
- Nombra los compuestos escribiendo al final del nombre con numeros romanos la valencia atomica del elemento con el nombre especifico. Ejemplo:
- Fe2+3S3-2 Sulfuro de Hierro (III).
- Oxisales
son compuestos formados por un metal, un no metal y oxígeno. Son consideradas como las sales de los ácidos oxoácidos, ya que éstas se forman por la sustitución de los hidrógenos del oxoácido por un metal.Nomenclatura de las oxisales
Nomenclatura tradicional: se nombra de forma similar al ácido oxoácido del que procede sustituyendo la terminación -oso por -ito y la terminación -ico por -ato seguido del elemento metálico terminado en:
- -ico (si tiene una valencia)
- -oso, -ico (si tiene 2 valencias)
- hipo...oso, -oso, -ico (si tiene 3 valencias)
- hipo...oso, -oso, -ico, per...ico (si tiene 4 valencias)
Ejemplos:
NaClO2 procede el ácido cloroso (HClO2), sustituimos -oso por -ito seguido del elemento metálico terminado en -ico porque sólo tiene una valencia, por lo tanto su nomenclatura tradicional es clorito sódico.
Nomenclatura de stock: se nombra de forma similar a la nomenclatura tradicional seguido del elemento metálico indicando la valencia con la que actúa en números romanos entre paréntesis.
Ejemplos:
Fe2(S04)3 sulfato de hierro (III)
Nomenclatura sistemática: se nombra con el nombre del anión seguido por el nombre del catión y seguido por el prefijo que indica el numero de átomos del elemento metálico. En el caso de que el anión se encuentre entre paréntesis, el número de iones se indica mediante los prefijos griegos:
- Para 2: bis-
- Para 3: tris-
- Para 4: tetrakis-
- Para 5: pentakis-
- Para 6: hexakis-
- Para 7: heptakis-
- Para 8: octakis-
- ...
Ejemplos:
Actuando el hierro con valencia 2:
FeSO2 dioxosulfato (II) de hierro
Biografías o fuentes de ayuda:
https://es.wikipedia.org/wiki/%C3%93xido_b%C3%A1sico.https://es.wikipedia.org/wiki/Hidruro.
https://es.wikipedia.org/wiki/Hidr%C3%B3xido
http://www.formulacionquimica.com/oxoacidos/
http://www.formulacionquimica.com/oxisales/
